Существует несколько возможностей лечения рака простаты с одинаково хорошими прогнозами. Поэтому решение каждого пациента сводится к вопросу: «На какие побочные эффекты я бы вероятнее всего согласился?» О разных методах лечения предстательной железы и их последствиях журналу Quora рассказывает доктор Гари Ларсон, медицинский директор Центра протонной терапии, Оклахома, США:
 — Американская Урологическая Ассоциация периодически проверяет все опубликованные материалы с результатами лечения рака простаты и всегда приходит к одному заключению – в целом нет разницы в вероятности излечения, будь то хирургия или лучевая терапия. Если бы один метод лечения явно превосходил все другие, это упростило бы жизнь. Мы, как врачи, тогда бы выбирали именно его. А так как проценты излечимости одинаковые, мужчинам все же необходимо обдумать все варианты и решить, какое лечение им выбрать (или, скажем так, против какого лечения они бы меньше всего возражали).
— Американская Урологическая Ассоциация периодически проверяет все опубликованные материалы с результатами лечения рака простаты и всегда приходит к одному заключению – в целом нет разницы в вероятности излечения, будь то хирургия или лучевая терапия. Если бы один метод лечения явно превосходил все другие, это упростило бы жизнь. Мы, как врачи, тогда бы выбирали именно его. А так как проценты излечимости одинаковые, мужчинам все же необходимо обдумать все варианты и решить, какое лечение им выбрать (или, скажем так, против какого лечения они бы меньше всего возражали).
Прежде чем продолжить, нужно иметь в виду следующие вещи.
Не все, у кого есть рак простаты, нуждаются в лечении – для многих мужчин будет достаточно активного наблюдения, по крайней мере, в течение короткого периода, а вероятно и всей жизни.
Есть только два метода лечения рака простаты – хирургический и лучевая терапия. Такие вещи как криотерапия, фокусированный ультразвук высокой интенсивности, прогревание микроволновым излучением, лазерная абляция и некоторые другие методы могут быть рекомендованы для рака простаты, повторно появившегося после прохождения основного лечения. Но сами по себе они не могут являться основным лечением.
Андрогенное подавление (гормональная терапия) остановит развитие большинства случаев рака простаты, снизит показатель ПСА практически до нуля и сократит новообразования и метастазы в кости, но его эффект будет только временным – от нескольких месяцев до нескольких лет. Как и методы, указанные выше, это само по себе не радикальное лечение, хотя оно может сочетаться с лучевой терапией для повышения вероятности излечения. Андрогенное подавление имеет набор побочных эффектов, включая усталость, потерю мышечной массы, набор веса, потерю либидо, импотенцию, остеопороз и депрессию.
Урологи любят говорить пациентам: «Если вы пройдете хирургическую операцию, вы всегда сможете после нее получить облучение. Но если вы сначала пролечитесь лучевой терапией, то потом вы не сможете пройти хирургическую операцию». По большей части, это является правдивым утверждением, но данное обобщение упускает некоторые определенные факты.
Во-первых, после лучевой терапии редко возникает необходимость проводить хирургическое вмешательство, так как большинство мужчин, не излечившихся от этой болезни, не имеют рецидивов в простате. Наоборот, при рецидивах после лучевого лечения рака простаты в большинстве случаев обнаруживаются злокачественные опухоли в других органах. Как правило, такие пациенты имели скрытое онкозаболевание помимо простаты, которое нельзя было определить до начала лечения. Скоплениям раковых клеток необходимо разрастись до определенных размеров, чтобы они смогли вызвать повышение показателя ПСА и стали заметными.
Если у пациента после лучевой терапии постоянно отмечается повышенный уровень ПСА, а повторные биопсии железы положительные (между прочим, результаты биопсии являются надежными только спустя два года после лучевой терапии, так как раковые клетки отмирают в течение какого-то времени после лечения), то шансы на рецидив только в железе составляют 50%.
Спасительная в этом случае простатэктомия может быть выполнена после лучевой терапии, хотя это трудная операция из-за интенсивного фиброза вокруг железы и пониженного кровообращения – оба состояния являются результатом перенесенной лучевой терапии. Такие операции лучше всего проводить в крупном урологическом центре, где проводится большое количество подобных вмешательств, вместо того, что доверить эту операцию урологу небольшой клиники. Но даже при высоком мастерстве хирурга существует высокий риск возникновения недержания вследствие простатэктомии, проведенной после лучевой терапии.
Так как риск возникновения рецидива рака только в простате составляет 50 на 50, то и шансы на то, что хирургия приведет к излечению также 50 на 50.
Если первичной была хирургическая операция, то в 20-30% случаев после нее пациент должен пройти лучевую терапию для полного излечения. Послеоперационная лучевая терапия дает 90-процентный шанс ликвидации любого оставшегося рака. Кстати говоря, когда хирурги называют общий процент исцелившихся пациентов, они включают в это число и тех мужчин, которые были вылечены только благодаря послеоперационной лучевой терапии, хотя редко упоминают об этом факте в своих публикациях.
Рак простаты обычно растет медленно. Термин «ранняя стадия» имеет отношение к тому факту, что он все еще локализован в простате или, как минимум, в ближайшей перипростатической ткани. Ранняя стадия также может быть низкого, среднего или высокого риска по шкале Глиссона. Уровень риска определяется врачом после обследования материала биопсии по уровню ПСА и в некоторой степени по количеству положительных образцов биопсии.
Хирургическое лечение и последствия
В целом есть два метода выполнения простатэктомии. Открытая – когда хирург делает разрез от лобковой кости до пупка, вырезает простату и некоторые лимфоузлы, потом присоединяет шейку мочевого пузыря к оставшейся уретре (так как промежуточной уретры простаты уже нет) и оставляет катетер на месте на несколько недель для того, чтобы все зажило. Второй способ — роботизированная простатэктомия. Это практически та же самая операция, но выполняется через маленькие разрезы с использованием дистанционно управляемых роботизированных манипуляторов и стереоскопической визуализации. В опытных руках диссекция является более точной и сроки пребывания пациента в больнице короче. В публикациях сообщается о потенциально возможном снижении побочных эффектов, таких как инфекция и кровотечение, но трудно сказать что-то определенное об осложнениях в долгосрочной перспективе, таких как импотенция и недержание.
Основной побочный эффект, который имеет хирургия и которого нет у лучевой терапии, — это недержание. Большинству мужчин требуется от одного до двух месяцев, чтобы восстановить регуляцию функции мочеиспускания, а около 5% прооперированных никогда не восстанавливают контроль над мочеиспусканием, им приходится использовать памперсы до конца жизни.
Импотенция встречается чаще при хирургии по сравнению с лучевой терапией. Хотя хирургические издания часто сообщают о сохранении потенции на уровне выше 50%, они определяют потенцию как «способность получать эрекцию, достаточную для вагинального проникновения». Поэтому если вы можете заниматься сексом в течение 30 секунд, урологи считают вас способным к половому акту.
Я обследовал первых 150 мужчин, которым я проводил брахитерапию в середине 1990-х и просто задал им такой вопрос: «Вы довольны вашей сексуальной жизнью?» Я оставлял им место на опросном листе для подробного ответа. Более 60% ответили, что они довольны их сексуальной функцией. И ни один из тех, кто сказал, что могут только достичь проникновения, не был доволен.
В нашем Протонном центре всякий раз при последующем приеме мы обследуем каждого мужчину, который прошел у нас лечение, при помощи двух средств оценки качества жизни. Первое из них — это опросный лист «Расширенный индекс рака простаты». А другой — анкета сексуального здоровья для мужчин. В нашей базе данных на данный момент более 2600 пациентов и оценки в баллах у более 70% из них показывают, что они удовлетворены своей сексуальной функцией.
В целом мужчины имеют гораздо лучшую сексуальную функцию и несравненно лучший контроль мочеиспускания (так число случаев недержания практически свелось к нулю – оно почти никогда не встречается при лучевой терапии), если они прошли лечение лучевой терапией, в отличие от хирургии.
Каковы минусы лучевой терапии?
Я коснусь этих моментов, так как они имеют отношение к каждому из различных способов, которыми проводится лучевая терапия.
Для пациентов с низким риском, локализованной болезнью (Глиссон 6 гистология с ПСА менее 10 и менее 4 позитивных образцов биопсии) брахитерапия может использоваться как монотерапия. Пациенты приходят для проведения процедуры разметки, при которой врачи определяют точный контур простаты каждые 5 мм сверху донизу, используя трансректальный ультразвук, а затем в компьютерной программе планирования лечения создают 3-D образ простаты. Рассчитывается оптимальная комбинация радиоактивных зерен, они заранее помещаются в иглы для введения их в железу. В день процедуры пациенту делается общая анестезия и используются от 20 до 40 игл для введения от 60 до 120 зерен в простату при помощи трансректального ультразвукового контроля.
Пациент обычно возвращается домой через несколько часов с катетером, установленным на ночь (так как железа может опухнуть, лучше установить катетер, чем ехать посреди ночи в больницу из-за проблем с мочеиспусканием). Мужчины обычно испытывают довольно серьезные неприятные симптомы, связанные с мочеиспусканием: частота позывов, неспособность терпеть, ночные позывы, сниженный напор струи, — которые проходят через месяц.
Пациенты могут иметь некоторые неприятные ректальные симптомы в течение нескольких недель. Может появиться ректальная язва в течение года или двух после процедуры лечения, если некоторые зерна оказались близко к ректальной стенке. Такая язва всегда заживает со временем, если только гастроэнтеролог не решит провести ее биопсию, заподозрив рак. В этом случае она может никогда не зажить, и пациенту понадобится колостомия.
Если у кого то есть факторы риска, кроме указанных выше, тогда одна только брахитерапия не даст достаточно высоких результатов излечения (вследствие того, что были затронуты перипростатические ткани вне пределов досягаемости радиационных зерен). Понадобится добавить двадцать пять процедур облучения внешней радиации для того, чтобы повысить дозу на перипростатические ткани. Основное преимущество брахитерапии — сокращение времени лечения — будет практически утрачено.
При заболевании от среднего до высокого риска, вероятно, придется выбрать внешнюю лучевую терапию как основной метод лечения, а не брахитерапию плюс сокращенный курс лучевой. Обычно курс лучевой терапии состоит курс из 44 процедур за девять недель.
Побочные эффекты внешней лучевой терапии как основного метода лечения рака простаты
Внешняя лучевая терапия может проводиться высокоэнергетическими рентгеновскими лучами, используя технику лучевой терапии с модулированной интенсивностью, или протонной терапией. Я сравню эти два метода. Кстати, Кибер-нож, томотерапия и другие разнообразные линейные ускорители проводят лечение лучевой терапией с модулированной интенсивностью при помощи рентгеновских лучей (фотонов). Между ними в конечном итоге разницы нет, отличаются только машины, которыми проводят лечение. Возможно, вы также слышали термин лучевая терапия с визуальным контролем, который просто означает, что проводится какое-то сканирование пациента на лечебном столе прямо перед проведением лечения. Это может быть КТ, портальное сканирование, стереоскопические рентгеновские лучи и др. Лучевая терапия с визуальным контролем используется со всеми формами лучевой терапии с модулированной интенсивностью, а также с протонной терапией.
Для обоих методов (протоны или фотоны) планирование лечения начинается с КТ сканирования тонкими слоями, которое интегрировано с высоко детализированной МРТ. КТ необходимо для того, чтобы сообщить компьютеру, планирующему лечение, толщину ткани во всех точках, через которые пройдет луч радиации. МРТ дает лучшую анатомическую картинку для определения контура простаты, семенных желез, мочевого пузыря, прямой кишки и т.д.
После нескольких дней, за которые создаются контуры органов, проводится множество опытов с конфигурацией луча, его модуляцией и т.д., вырабатывается оптимальный план лечения. После этого врач проводит проверку соответствия всем условиям для того, чтобы убедиться, что компьютерные расчеты дадут планируемое распределение дозы в ткани. И, наконец, пациент возвращается для первичного «визуального контроля» и первой из 44 процедур.
Радиолог — онколог встречается с каждым пациентом еженедельно и занимается побочными эффектами, которые могут возникнуть. В ходе лечения лучевой терапией с модулированной интенсивностью фотонами это может быть усталость, иногда до такой степени, что пациентам приходится идти домой и спать пару часов во второй половине дня.
После нескольких недель лечения может появиться ректальное раздражение, которое выражается в симптомах от слабой диареи до боли, кровотечения и постоянного ощущения в необходимости опорожнить кишечник, хотя в стуле может быть ничего, кроме небольшого количества слизи.
Также после нескольких недель лечения могут появиться раздражающие урологические симптомы, такие как частота походов в туалет, неспособность терпеть позывы, медленное опорожнение мочевого пузыря и необходимость несколько раз вставать ночью. Они могут длиться несколько недель после прохождения лечения.
Риски, которые могут возникнуть в будущем, включают развитие рака, вызванного радиацией. Кроме долгосрочного риска появления вторичного рака, большинство побочных эффектов проходят за срок от нескольких месяцев до года после окончания лучевой терапии.
Протонная терапия
При протонной терапии побочные эффекты выглядят иначе. Усталость минимальная или отсутствует вообще. (Я лечил одного заядлого велосипедиста, который проехал на своем велосипеде более тысячи миль за девять недель, во течение которых проходил терапию).
Ректальные симптомы почти не встречаются, так как только очень маленький объем прямой кишки получает радиацию. Урологические раздражающие симптомы могут появиться на такой же срок, как и при лечении рентгеновскими лучами (фотонами), хотя обычно они менее серьезны.
Множественные эпидемиологические исследования показали, что существует только минимальное повышение риска возникновения рака после облучения протонами по сравнению с рентгеновскими лучами. Вероятно из-за меньшего объема ткани, получающего какую-то дозу радиации. Если у мужчин и появляются немногие побочные эффекты, они обычно проходят за несколько недель после окончания облучения протонами.
Каковы сравнительные данные по побочным эффектам протонной терапии против лучевой терапии с модулируемой интенсивностью?
Мы объединили наши данные с различными онкологическими центрами, обследовали приблизительно 1000 пациентов, которые прошли лечение рака простаты протонной терапией, и сравнили их показатели качества жизни с мужчинами из контрольной группы, которые не проходили лечение (потому что у не было рака простаты).
Все мужчины заполняли опросные листы касательно качества их жизни каждые три месяца с начала лечения до, как минимум, одного года после лечения. Результаты показали, что пациенты, которые прошли лечение протонной терапией, имели такие же показатели качества жизни, как и те, у которых даже не было рака простаты.
Рак простаты обычно растет медленно. Не позволяйте никому подгонять вас при принятии решения, которое будет иметь последствия до конца вашей жизни.
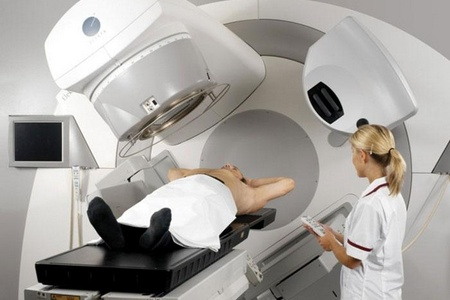
Лучевая терапия при раке простаты

На сегодняшний день злокачественная опухоль простаты у мужчин разной степени тяжести ─ одна из самых распространенных причин летального исхода от онкологии. Среди самых эффективных методов локальной терапии злокачественной опухоли простаты – лучевая терапия.
Применяют данный способ лечения на начальной стадии патологии, а также в случае, когда нет возможности назначить простатэктомию, либо пациент категорически против такого варианта терапии. В более сложных случаях ее проводят в сочетании с лечением гормональными препаратами.
Особенности терапии
Медицинские исследования давно подтвердили, что лучевая терапия онкологии простаты ─ эффективный метод лечения патологии. У этого метода есть другое название – радиотерапия, в основе которого лежит воздействие на пораженный орган ионизирующей радиацией.

Лучи воздействуют исключительно на патогенные клетки. При этом в ходе процедуры здоровые не затрагиваются. Лучевая терапия может быть рекомендована на любой стадии рака простаты.
Излучение выполняют несколькими способами: волновым и корпускулярным. Гамма- или рентгеновские лучи вырабатываются в первом случае. При втором типе воздействие производят с помощью:
- Альфа-частиц.
- Электронного излучения.
- Нейтронного излучения.
- Бета-частиц.
- Протонного излучения.
Лечебную радиацию активно используют для борьбы с онкологией простаты на любой стадии патологии. Радиотерапию применяют как хирургический, так и профилактический метод. Облучение по эффективности сравнивают с полостной операцией по удалению новообразования.
Показания для проведения
Специалисты рекомендуют проведение радиотерапии простаты следующим пациентам:
- Больным, которым противопоказано хирургическое вмешательство. К примеру, это может быть связано с возрастом или патологией сердечно-сосудистой системы. В этом случае лучевую терапию осуществляют без использования анестетиков. Благодаря этому сердечная мышца и остальные органы не испытывают лишнюю нагрузку.
- В случае, когда злокачественная опухоль в простате распространилась за пределы капсулы железы, и специалист не видит смысла в проведении операции (на последних стадиях онкологии). В этом случае применяют экзогенную радиотерапию.
- В случае, если после проведения простатэктомии у пациента обнаружена быстро разрастающаяся опухоль с метастазированием, а также при высокой вероятности рецидива онкологии врач может рекомендовать проведение облучения ложа простаты.
Разновидности лучевой терапии
В арсенале современных онкологов имеется несколько видов лучевой терапии:
- Дистанционная.
- Брахитерапия.
- Протонная.
- Контактная лучевая терапия.
Специалист подбирает наиболее эффективный вариант индивидуально, исходя из стадии диагностируемого онкологического очага, его размеров, структуры, присутствия метастазов в других органах, состояния здоровья мужчины, его восприимчивости к назначенному лечению.
Дистанционная лучевая терапия

Определив точную локализацию и размеры злокачественной опухоли с помощью МРТ и КТ диагностики, специалисты чаще всего рекомендуют проведение дистанционного варианта облучения. Сохранить целостность органов и тканей, еще не пораженных мутированными клетками, окружающих очаг, – главная цель терапии.
Как правило, процедуры проводят в условиях стационара. Лечебный курс длится как минимум два месяца. После проведенной терапии проводят анализ состояния здоровья больного, делают перерыв, чтобы здоровые ткани восстановились.
Основные преимущества:
- Процедуру проводят в амбулаторных условиях.
- Минимальный риск развития тяжелых осложнений и последствий.
- Отличная переносимость пациентами.
Но, как и любой метод лечения, этот способ имеет свои недостатки, которые заставляют специалистов сомневаться в целесообразности этой терапии:
- Развитие лучевых язвенных дефектов.
- Высокая вероятность поражения радиацией органов и систем, соседствующих с простатой.
- Возможные нарушения в системе свертывания крови.
После тщательного анализа всех результатов предварительных диагностических процедур лечащий врач принимает решение о целесообразности применения дистанционного облучения.
Протонная

Протонное облучение железы – вид лучевой терапии, который имеет минимальные побочные эффекты. Принцип воздействия обусловлен тем, что облучение злокачественных клеток происходит на молекулярном уровне. Фактически протоны разрушают ДНК. При этом дозы облучения минимальные, воздействие на здоровые ткани ограничено. После процедуры новообразование перестает расти, а клетки не размножаются.
Преимущества протонного облучения:
- Небольшие радиационные дозы.
- Одинаковая эффективность, независимо от локализации опухоли.
Протонную терапию назначают даже детям с онкозаболеваниями, так как дозы облучения незначительны. Метод наиболее подходит для продолжительного лечения при борьбе с метастазированием. После облучения этим методом риск рецидива онкологии снижается на 10%.
Брахитерапия
Самая распространенная методика лучевой терапии, которая отличается высокой эффективностью. Обладает минимальной степенью травматизма органов, окружающих простату.
После определения размеров и структуры ракового новообразования в него устанавливается радиоактивный компонент – воздействие радиации на органы и ткани, окружающие опухоль, сведено к минимуму. На сегодняшний день применяют внутрисосудистую, внутриполостную либо внутритканевую брахитерапию.

Проявление тяжелых осложнений и негативных эффектов после применения любого из методов сведено к минимуму. Процедуру отлично переносят пациенты преклонной возрастной категории.
Могут проводить временную брахитерапию: во время процедуры в железу вводят полую иглу, впоследствии заполняя ее радиоактивной жидкостью. Спустя примерно десять минут иглу вынимают, а оставшаяся жидкость начинает контактировать с мутировавшими частями органа. Несколько подобных манипуляций выполняют на протяжении четырех суток.

Возможна и длительная брахитерапия: в орган под контролем аппарата УЗИ внедряют радиоактивный имплант. Высокие целенаправленные дозы радиации воздействуют исключительно локально на определенную область железы, не воздействуя на соседние ткани.
К преимуществам методики относят:
- Высокая эффективность.
- Большой процент выживаемости – до 75–80%.
- Минимальный риск развития последствий.
- Быстрая реабилитация.
- Уже на следующий день после завершения процедур пациент может отправиться домой.
Возможные недостатки методики:
- Дизурические расстройства.
- Не слишком сильное, но жжение при мочеиспускании.
- Небольшая затрудненность с мочеиспусканием или недержание.
- В редких случаях может появиться кровотечение из ануса.
Только высококвалифицированный специалист может назначить брахитерапию. Считается, что данная процедура – лучшая альтернатива простатэктомии, которая считалась единственным способом борьбы с онкологией органа.
Контактная лучевая терапия
Данный метод выполняют внутриполостно, аппликационно и внутритканево. В любом случае происходит прямое воздействие на патологические клетки.
Для лечения онкологии простаты применяют только внутриполостной и внутритканевый методы. При первом методе радиоактивный источник в форме шариков, бусинок либо капсул вводят в прямую кишку или мочевой пузырь пациента и фиксируют там, в области злокачественной опухоли. При внутритканевом методе нитевидные или игловидные радиоисточники вводят непосредственно в опухоль.
В качестве наружных методов радиотерапии могут применять конформную лучевую терапию онкологии простаты с использованием трехмерной (3D) съемки мочевого пузыря, простаты и прямой кишки. Это помогает не только повысить дозу облучения раковых клеток, но и снизить вероятность облучения соседних органов, благодаря чему эффективность терапии значительно повышается.
Противопоказания
Лучевая терапия противопоказана в таких случаях:
- Язвенный колит, диарея и прочие патологии прямой кишки у пациента.
- Ранее проведенное облучение малого таза.
- Наличие ожирения 3-4 степени.
- Присутствие крови в моче.
- Азотемия (повышенный креатинин крови).
- Проблемы с мочеиспусканием.
Лучевая терапия раковой опухоли простаты – достаточно эффективное современное средство. Однако необходимо учитывать и опасность радиоактивного облучения для организма. Перед назначением данного лечения специалист должен провести всестороннее исследование.
Возможные последствия
Негативные последствия в ходе лучевой терапии при онкологии простаты наблюдаются достаточно часто. Это один из существенных недостатков лечения. Пациенты, прошедшие курс лечения, свидетельствуют о том, что состояние в период терапии и после нее может ухудшиться.
Больной может испытывать следующие негативные последствия:
- Тошнота
- Потеря аппетита
- Рвота
- Депрессивное состояние
- Нарушения сна
- Усталость, слабость и плохое самочувствие.
Многие пациенты отмечают появление значительных проблем с ЖКТ, которые выражаются в виде диареи, запоров и вздутия. Соблюдение диеты позволит быстро избавиться от неприятных симптомов. Лучевое облучение может спровоцировать учащение мочеиспускания, однако через определенный промежуток времени состояние нормализуется. У некоторых пациентов патология приобретает хроническую форму. В некоторых случаях может наблюдаться недержание урины.
Лучевая терапия оказывает влияние на эректильную функцию, которая при длительной терапии может перерасти в импотенцию.

За счет ослабления иммунной системы организм мужчины более подвержен возникновению заболеваний инфекционного характера. В этот период бактерии и вирусы наиболее сильно воздействуют на организм.
У многих пациентов наблюдаются сухость слизистых оболочек рта, глаз, выпадение волос. В каждом конкретном случае реакции могут быть индивидуальными. Сразу же после прекращения воздействия радиации состояние может нормализоваться, либо же побочные эффекты могут наблюдаться на протяжении некоторого времени после завершения терапии.
Период реабилитации
Чтобы организм полностью избавился от патогенных клеток и восстановился после лечения, требуется соблюдать определенные правила.
- Пациент должен соблюдать полный покой. Размеренный распорядок дня, который включает длительный сон и отдых ─ крайне важное условие в период реабилитации.
- Организм должен в полной мере насыщаться кислородом. Прогулки на свежем воздухе будут крайне полезны.
- По завершении терапии необходимо принимать препараты, повышающие иммунитет.
- Рекомендуется придерживаться принципов здорового питания, исключив тяжелую пищу. Важно питаться дробно, небольшими порциями.
- Физические нагрузки, курение, употребление спиртного, а также самолечение категорически запрещены.
В большинстве случаев уже спустя полгода после терапии наблюдается выздоровление. В этот период нужно регулярно сдавать анализы на ПСА. Обязательно необходимо строго соблюдать все рекомендации специалиста.

 432603
432603
Особенности лучевой терапии при раке простаты и ее последствия
В современном мире одной из наиболее часто встречающихся локализаций злокачественной опухоли у мужчин является рак предстательной железы различной степени тяжести, который является одной из распространенных причин смертности от рака. Данный вид злокачественных новообразований занимает второе место в структуре заболеваемости раком у мужчин в России (12,1 %), уступая только раку легкого, при этом среднегодовой темп прироста заболеваемости (8,45 %) является самым высоким среди всех злокачественных опухолей. В последние годы во всех онкологических медицинских заведениях России была внедрена программа ПСА-скрининга для простаты, благодаря которой появилась возможность диагностировать рак предстательной железы на начальных стадиях заболевания, что позволило значительно повысить процент выживаемости, предложить оптимальное лечение и добиться полного выздоровления пациентов с данным заболеванием. Лучевая терапия при раке предстательной железы является одним из основных и самых эффективных методов локального лечения злокачественной опухоли простаты. Последствия такой терапии поддаются лечению и возникают не всегда.
- Особенности терапии
- Когда используется
- Возможные последствия
Особенности терапии
К лучевой терапии простаты относятся внутритканевая брахитерапия имплантируемыми источниками с низкой мощностью дозы, внутритканевая брахитерапия источниками с высокой мощностью дозы, а также другие менее распространенные методики. Остановимся подробнее на особенностях лучевой терапии в борьбе с раком простаты и на степени тяжести последствий, которые может иметь это лечение для организма мужчины.
Лучевая терапия при раковых заболеваниях любой локализации может использоваться как основной метод борьбы с опухолью, так и быть частью других методик, которых в настоящее время разработано и опробовано достаточно много. Это лечение может использоваться в обеспечении быстрейшего выздоровления пациента, перенесшего операцию по удалению злокачественной опухоли предстательной железы, такую как простатэктомия.
Решение о применении лучевой терапии может принять только специалист после тщательной диагностики, изучения анамнеза и бесед с больным, учитывая уровень и динамику ПСА. Он же определяет, какое именно лечение, в данном случае облучение, будет наиболее эффективным для каждого конкретного пациента.
Внимательный подход к схеме лечения обусловлен в первую очередь тем, что лучевая терапия (облучение) при лечении любой злокачественной опухоли, в том числе и рака простаты, может иметь не только положительный эффект, но и вызвать многочисленные виды негативных последствий различной степени тяжести для ослабленного организма. Доза допустимого безопасного облучения для человека строго определена, но индивидуальную реакцию больного на такое лечение специалист предугадать не может.
 Проводить лечение рака простаты необходимо только под контролем врача.
Проводить лечение рака простаты необходимо только под контролем врача.
Проводить лечение рака простаты методом лучевой терапии можно только в стационаре, контролирует все лечащий врач – специалист в этой области, причем положительного эффекта можно добиться в результате проведения нескольких лечебных курсов с интервалом порядка полугода под контролем ПСА.
Задайте вопрос врачу-урологу!

Когда используется
Лучевая терапия при раке простаты может быть использована как основной метод воздействия на злокачественное образование, если болезнь была обнаружена на начальной степени развития. Первая и вторая стадии рака не всегда требуют хирургического вмешательства, но в этой степени болезни простатэктомия бывает максимально эффективной. При дальнейшем развитии опухоли, в третьей и четвертой степени, хирургическое лечение часто уже бывает невозможно или бесполезно. При этой клинической картине лучевая терапия способна остановить рост раковых клеток и разрастание метастазов. На этих стадиях данный метод терапии может быть эффективным дополнением к химиотерапии. Контроль осуществляется по динамике ПСА. В зависимости от размеров и формы опухоли оптимальные дозы радиационного воздействия специалист определяет строго индивидуально. Простатэктомия дополняется лучевой терапией после гистологического исследования новообразования предстательной железы.
Лучевая терапия назначается с большой осторожностью при распространении метастазов в костную ткань, поскольку может вызвать дополнительные осложнения. Несмотря на то что при применении данного метода значительно снижается болевой синдром, он сильно влияет на количество кровяных клеток. Снижение количества этих клеток далеко не единственный побочный эффект радиационного воздействия на человеческий организм. Высоких результатов в лечении рака простаты добились врачи Центра простаты Университетской больницы Арау в Швейцарии, показатели здесь лучшие в мире.
Перед назначением больному лучевой терапии врачу необходимо провести пробную диагностику для определения индивидуальной дозы радиационного воздействия и обозначить количество необходимых сеансов для того, чтобы лечение было не только эффективным, но и максимально безвредным, т. е. минимизировать случаи возникновения серьезных осложнений и степень негативного влияния на организм. Важен на этом этапе показатель ПСА. Также надо определить, нужна ли дополнительно какая-то операция.
 Вид лучевой терапии определяет врач, исходя из предварительной диагностики состояния пациента.
Вид лучевой терапии определяет врач, исходя из предварительной диагностики состояния пациента.
В настоящее время онкологами используются различные виды лучевой терапии простаты, имеющие различное воздействие на злокачественное образование и последствия. Выделим основные из них:
- Дистанционная.
- Протонная.
- Брахитерапия.
- Контактная лучевая терапия.
Подходящую конкретному пациенту методику определяет лечащий врач по результатам проведенных предварительных исследований, в том числе ПСА, он делает назначение, при котором осложнения будут минимизированы, а также подбирает определенную диету, обеспечивающую полноценное питание ослабленного организма.
Возможные последствия
Любое лечение рака простаты влечет за собой последствия, иногда они незначительны, а порою доставляют массу неудобств пациенту.
- Изменения в мочеиспускании.
Облучение может стать причиной такого осложнения, как некоторое раздражение и отек предстательной железы. Предстательная железа располагается рядом с уретрой (трубкой, которая соединяет мочевой пузырь с внешним миром). При отеке предстательной железы может создаваться давление на уретру, и возникают следующие последствия:
- Затрудненное начало мочеиспускания.
- Ослабление потока мочи при мочеиспускании.
Может возникать чувство невозможности терпеть позыв к мочеиспусканию; либо возникает ощущение неполного опорожнения мочевого пузыря, которое провоцирует:
- Более частое мочеиспускание.
- Многократные подъемы ночью, чтобы помочиться.
Иногда больные после лучевой терапии замечают кровь в моче.
При наличии любого из перечисленных симптомов последствий больному необходимо срочно обращаться к лечащему врачу, который подберет препараты для их облегчения.
- Жжение при мочеиспускании.
Облучение может оказывать раздражающее воздействие на мочевой пузырь и уретру (трубка, которая выводит мочу из мочевого пузыря и организма). Такое последствие встречается часто. Это может вызывать жжение при мочеиспускании. Подобное состояние называется цистит, случаи возникновения его после лучевой терапии предстательной железы встречаются с большой частотой. При возникновении цистита больному рекомендуется увеличить количество потребляемой жидкости. Дополнительное питье способствует увеличению содержания воды в моче и снижению раздражающего действия на уретру. При длительном течении цистита необходимо провести исследование мочи для выявления возможной инфекции мочевого пузыря. При обнаружении инфекции врач обычно назначает курс антибиотиков, а в случае ее отсутствия – препараты для уменьшения чувства жжения.
 Диарея возникает при попадании толстого кишечника или толстой кишки в зону воздействия лучевой терапии.
Диарея возникает при попадании толстого кишечника или толстой кишки в зону воздействия лучевой терапии.
- Диарея.
Диарея возникает при попадании толстого кишечника или толстой кишки в зону воздействия лучевой терапии. Клетки кишечника делятся довольно быстро и в большей степени подвержены действию облучения. Вследствие этого могут возникнуть такие последствия, как спазмы в животе или диарея. Обычно этот эффект наблюдается через 10-14 сеансов лечения. У некоторых пациентов диарея появляется раньше, а некоторых она минует. Чтобы уменьшить негативное воздействие облучения на кишечник, врач обычно рекомендует пациенту выпивать по 3-4 стакана воды за 30 минут до каждого сеанса лечения, чтобы наполнить мочевой пузырь, а также питание по особой диете. Когда мочевой пузырь полон, он поддавливает кишечник и помогает сместить его из зоны лечения. Это должно помочь уменьшить спазмы в животе и диарею. Также очень важную роль в борьбе с диареей имеет правильное питание.
Диарея в сочетании с облучением может вызвать раздражение и болезненность кожи вокруг ануса. При появлении болезненности кожи следует отказаться от использования туалетной бумаги. В качестве замены можно воспользоваться детскими или другими мягкими влажными салфетками в качестве средства гигиены после дефекации.
- Утомление.
Утомление является распространенным последствием, однако может проявляться у пациентов в различной степени. Стресс на фоне рака предстательной железы, ежедневные поездки для прохождения лечения, а также последствия воздействия облучения на здоровые клетки могут вызывать у больного чувство большей усталости. Обычно утомление появляется после 10 сеансов лечения. Может показаться, что оно усиливается к концу недели, но проходит после выходных. Утомление может сохраняться от нескольких недель до нескольких месяцев после окончания курса лечения. Активные мероприятия следует планировать на начало недели, когда ощущается прилив энергии. Больному рекомендуется придерживаться режима и вставать в одно и то же время 7 дней в неделю, вести активный образ жизни и по возможности делать зарядку. Важно не перегружать себя. При появлении признаков усталости следует запланировать периоды отдыха в течение дня. Важную роль в борьбе с утомлением играет правильное питание.
- Эректильная дисфункция.
Обычно эректильную дисфункцию вызывает операция – простатэктомия, как осложнение сразу после лучевой терапии она встречается достаточно редко, но может развиться постепенно. Лечение данного осложнения бывает достаточно эффективным при применении различных лекарственных трав.
Случаи полного излечения пациентов с раком предстательной железы различной степени после лучевой терапии имеют тенденцию к увеличению. Отзывы больных, прошедших данное лечение, самые позитивные, осложнения после такого лечения относительно небольшие. Ни в коем случае нельзя пренебрегать помощью врача-онколога при самых первых проявлениях симптомов заболевания, регулярно выполнять контроль ПСА. При назначении курса лучевой терапии необходимо строго следовать врачебным рекомендациям, а в реабилитационном периоде помнить, что правильное питание, отказ от вредных привычек, регулярное посещение врача-онколога являются залогом полного излечения. Одних из высоких показателей в мире по лечению рака простаты добилась клиника Арау в Швейцарии.
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.
Виды и последствия лучевой терапии при раке предстательной железы
Онкология тяжело поддается медикаментозному лечению. Курс терапии часто включает в себя несколько способов уничтожения раковых клеток. Радиотерапия рекомендуется в комплексе с химиотерапией и оперативным лечением. Последствия лучевой терапии при раке предстательной железы многообразные, несмотря на то, что современные методы облучения уменьшили пагубное воздействие на организм человека. Рассмотрим, кому необходима данная процедура, и как уменьшить отрицательные явления от облучения?
- 1 Когда необходимо делать облучение простаты?
- 2 Виды лучевой терапии при раке простаты
- 3 Побочные эффекты лучевой терапии
- 4 Уменьшение негативного влияния радиотерапии
- 5 Каковы противопоказания к проведению процедуры?
Когда необходимо делать облучение простаты?

При раке облучение простаты – это способ лечения, базирующийся на использовании ионизирующей радиации. В современной медицинской практике применяются методы, которые действуют направленно, то есть, только на опухоль.
Стоит знать: радиация целенаправленно уничтожает раковые клетки, при этом практически не воздействует на здоровые ткани. По эффективности манипуляцию можно сравнить с полостной операцией по иссечению опухолевого новообразования.
Лучевая терапия при раке простаты проводится в следующих случаях:
- На ранней стадии онкологического процесса, когда диагностируется рак первой либо второй стадии. Облучение может выступать моносредством, либо комбинироваться с хирургическим вмешательством.
- Воздействие радиацией осуществляется на 3-4 стадии ракового процесса, когда по ряду причин пациенту не могут сделать операцию.
- Лечение пациентов пожилой возрастной группы, которые имеют в анамнезе серьезные хронические заболевания – патологии сердца и кровеносных сосудов, дыхательной системы и пр. В этом случае риск от операции больше, чем от самой опухоли.
- Целесообразно проводить облучение на последней стадии рака вместе с химиотерапией и гормональным лечением. При наличии метастаз процедура помогает снизить болевой синдром.
- Проведение облучения после хирургического вмешательства, в ходе которого была удалена предстательная железа, помогает предупредить рецидив болезни и появление метастаз.
Перед лечением доктор должен выявить стадию рака простаты. Лучевая терапия на фоне отсутствия медицинских противопоказаний назначается незамедлительно.
Виды лучевой терапии при раке простаты

Первые эксперименты с радиоактивным излучением проводились в середине двадцатого века. Они показали высокий результат, но при этом выявились определенные минусы. В частности, это серьезное повреждение здоровых клеток, что приводило к целому спектру негативных симптомов.
Современные методики имеют мало общего с прошлыми пробами. Прорывом в терапии рака стало использование узконаправленного излучения. Иными словами, появилась возможность воздействовать исключительно на больной орган, что значительно увеличивает шансы на восстановление.
Стоит знать: все используемые методики лучевого облучения классифицируются на две большие группы – дистанционный способ (внешнее применение радиации) и ионизирующий вариант (влияние на опухоль изнутри). Ни один из применяемых методов не гарантирует 100% исцеление пациента. Для повышения эффективности терапии рекомендуется комбинированное облучение – совмещаются 2 и более способов радиотерапии.
Лучевая терапия аденомы простаты не осуществляется, поскольку гиперплазия предстательной железы является доброкачественным процессом. Целесообразно применять эту методику, если болезнь озлокачествляется, что маловероятно.
Дистанционная терапия подразумевает воздействие на опухоль вне тела пациента. Существует несколько методик проведения:
- Конвенциональный способ применяется чаще всего. В процессе манипуляции аппарату задаются определенные установки, вследствие чего осуществляется воздействие на опухоль под заданным углом;
- 3D-комформное лечение характеризуется предельной точностью влияния на опухолевое новообразование. К преимуществам метода относят малый список побочных эффектов, целенаправленность воздействия, слабое влияние на здоровые ткани. Для манипуляции применяется высокоточное оборудование;
- Метод IMRT расшифровывается как интенсивное лучевое модулированное лечение предстательной железы. Такой вариант способствует снижению негативного воздействия на др. внутренние органы;
- SBRT – стереотаксический способ терапии, предполагающий излучение непосредственно на очаг. Длительность лечебного курса менее семи суток;
- IGRT – облучение с коррекцией изображения. В ходе манипуляции удается получить картинку опухолевого новообразования либо сразу после нее. При этом доза радиации, получаемая нормальными клетками, сводится к нулю.

Отмечается, что внешнее влияние на рак простаты часто приводит к появлению ожога в месте проникновения, ломкости кровеносных сосудов, нередко появляются кровоизлияния.
Брахитерапия либо контактное лечение имеет неоспоримое достоинство – оказывается влияние именно на очаг. Вся манипуляция контролируется посредством аппарата ультразвукового исследования. Радиоактивные зерна вводят специальной иголкой через промежность.
Брахитерапия бывает нескольких типов в зависимости от времени воздействия:
- Продолжительная. В очаг образования вводят стержни, которые обогащены радиоактивным йодом. Выраженность облучения маленькая, но лечебный результат обусловлен постоянным влиянием.
- Временная. Процедура подразумевает введение в простату радиоактивного элемента с большой дозой излучения. Его оставляют внутри тела на малый промежуток времени, затем он извлекается. Это приводит к отмиранию патологических тканей, вследствие чего уменьшается размер простаты.
Дозировка облучения рассчитывается в соответствии с радиологическими схемами, таблицами и установленными международными нормами.
Еще один способ лечения – это протонное воздействие. Терапевтический эффект достигается благодаря влиянию на клеточном уровне. Протоны уничтожают онкологические клетки, при этом дозировка радиации очень маленькая, соответственно, вред для здоровой ткани сводится к минимуму. Вероятность того, что рак простаты после облучения протонным способом вернется, меньше на 10% в сравнении с др. методиками.
Побочные эффекты лучевой терапии

Последствия лучевой терапии при раке простаты всегда развиваются, несмотря на то, что современные методы стараются минимизировать отрицательные явления. Осложнения в основном обусловлены нарушением функциональности здоровых клеток. Они проявляются в течение 90 дней после манипуляции, либо возникают спустя продолжительный отрезок времени 3-24 месяца.
- Нарушение функциональности пищеварительного и желудочно-кишечного тракта, что проявляется жидким стулом, повышенным газообразованием, вздутием живота, отрыжкой и пр.;
- Проблемы с мочеиспусканием различной степени тяжести, в том числе и острая задержка мочи;
- Цистит (очаг воспаления в мочевом пузыре);
- Ректит – воспаление слизистой оболочки прямой кишки, которое сопровождается отечностью, покраснением, а в тяжелых случаях выявляется отторжение эпителия.
Важно: к отдаленным осложнениям, которые могут проявиться через долгое время, относят уретрит, поверхностный некроз уретры, лучевую форму фиброза, гидронефроз почек, импотенцию.
Повреждения прямой кишки развиваются относительно часто. Проблему игнорировать нельзя, требуется соответствующее лечение. Если не предпринимать никаких действий, это грозит летальным исходом. Что же касается жидкого стула, то в большинстве случаев работа ЖКТ нормализуется самостоятельно в течение небольшого периода времени – когда организм привыкнет к новому размеру предстательной железы.
Свободный выход мочи нарушается вследствие фиброзных изменений тканей. Данный процесс носит необратимый характер, поэтому нужно лечить как можно быстрее. Согласно статистике такое осложнение развивается через 1-2 года после лучевой терапии.
Нарушение эректильной функции после лучевой терапии предстательной железы наблюдается у многих мужчин. Для лечения используют стимуляторы (Виагра), инъекции в половой член, а в запущенных случаях применяются имплантаты.
Уменьшение негативного влияния радиотерапии

Несмотря на многочисленные ранние и отсроченные осложнения, лучевая терапия применяется достаточно часто, поскольку помогает уничтожить злокачественные клетки и не дает им размножаться; способствует закупориванию кровеносных сосудов, вследствие чего опухоль не растет, так как не получает питательные вещества.
Врачами разработаны мероприятия, помогающие снизить пагубное воздействие на организм:
- Исключить из меню алкогольные напитки, отказаться от вредных привычек. Пациенту нужно правильно и сбалансировано питаться, уделяя особое внимание фруктам, овощам, растительной клетчатке.
- Тщательное соблюдение гигиены промежности.
- Перед терапией нужно обязательно проверить больного на наличие инфекционных патологий мочеполовой системы. Если у пациента цистит либо пиелонефрит, перед облучением требуется антибактериальное лечение.
- Если у мужчины проблемы с мочеиспусканием, то лечение онкологии начинают с гормональных препаратов, после присоединяют радиоактивное излучение, которое начинают с минимальной дозировки.
- Перед манипуляцией требуется отказаться от любого воздействия механического характера на уретральный канал.
- Когда пациент находится в тяжелом состоянии, между этапами облучения нужно выдержать перерыв 14-21 день.
- При первых симптомам ректита как следствия медицинской манипуляции, нужно применять ректальные суппозитории с красавкой, метилурациловые свечи, проводить клизмы на основе лечебных масел.
Совет: чтобы минимизировать осложнения лучевой терапии в первые 2 месяца нельзя поднимать предметы, тяжелее 4-х кг; не рекомендуется сидеть более двух часов подряд; надо постоянно следить, чтобы кишечник и мочевой пузырь не были переполнены.
Каковы противопоказания к проведению процедуры?
Радиотерапия не может назначаться всем пациентам, у которых диагностировали онкологию предстательной железы. У манипуляции имеются прямые противопоказания. При назначении облучения обязательно учитывают общее состояние пациента.
- Если у пациента установлен катетер для отвода урины;
- Наличие воспалительного процесса в организме. Особенно, когда у больного обострение цистита или ректита;
- В анамнезе воздействие радиацией на органы малого таза;
- Ожирение третьей и четвертой степени;
- Хронический понос;
- Высокая концентрация креатинина в крови;
- Тяжелое состояние больного.
Прежде чем назначить лучевую терапию обязательно учитывают вероятные негативные последствия после оной. Больной, который находится в критическом состоянии, не сможет справиться с осложнениями, что заканчивается смертью.
Использование радиотерапии значительно увеличивает шанс пациента с раком на жизнь, особенно на раннем этапе патологического процесса. Когда заболевание запущено, лучевое лечение позволяет продлить жизнь на долгое время и улучшить ее качество.
Лучевая терапия при раке предстательной железы
Лучевая терапия при раке простаты — применение ионизирующего излучения в медицинских целях для замедления прогрессирования или искоренения злокачественного новообразования. Выделяют три основных варианта радиотерапии: чрескожную, низкодозную и высокодозную брахитерапию. Последствия лучевой терапии при раке предстательной железы зависят от опыта врача и состояния здоровья пациента.
Содержание
Механизм действия лучевой терапии
Основная цель радиотерапии — повреждение малигнизированных клеток ионизирующим излучением с минимальным влиянием на здоровые окружающие ткани. В клинической практике используют различные типы излучения от различных источников, например рентгеновское и гамма. Место опухоли визуализируется в виде трехмерной компьютерной модели из результатов компьютерной или магнитно-резонансной томографии. Распределение лучей можно спланировать таким образом, чтобы минимальная доза (для рака простаты 74–80 Гр) достигалась во всей малигнизированной ткани с минимальным влиянием на чувствительные к радиации органы — мочевой пузырь и кишечник. Различают терапевтическую и паллиативную лучевую терапию. Последняя используется для облегчения симптомов, возникающих на терминальных стадиях. При раке простаты терапевтическая форма применяется в качестве альтернативы хирургии — радикальной простатэктомии.

Чрескожная лучевая терапия
Это основной вариант лечения локально-ограниченного рака предстательной железы всех групп риска. Облучение через кожу также называется внешней лучевой терапией и проводится амбулаторно без анестезии.
Конформная. При конформной чрескожной радиотерапии проводится трехмерное планирование выбранного объема облучения, что уменьшает риск развития поздних осложнений. Местоположение и объем радиации постоянно измеряются и корректируются при необходимости. Чтобы больше повредить опухоль и защитить здоровые ткани, общая доза также делится на несколько отдельных доз (фракций). Обычно используется 1,8–2,0 Гр пять дней в неделю, или 70 Гр — за 7–8 недель.
ДС модуляцией интенсивности. Другой вариант — радиотерапия с модуляцией интенсивности излучения, которая позволяет использовать более высокую разовую дозу. Она может применяться для сокращения продолжительности лечения (например, 74–80 Гр в 28 дозах по 2,5 Гр каждая) или при неэффективности предыдущей лучевой терапии. Преимущество метода заключается в более высокой дозе облучения с уменьшенными побочными эффектами. Облучение должно происходить с использованием методов визуализации.
Низкодозная и высокодозная брахитерапия
Брахитерапия — это контактная радиотерапия, при которой радионуклид (радиоактивный химический элемент) вводится непосредственно в предстательную железу. Введение радиоактивного вещества проводится во время амбулаторного или кратковременного пребывания в стационаре под спинальной анестезией — с помощью полых игл, которые проталкиваются в предстательную железу из промежности под контролем трансректального ультразвукового исследования.
Низкодозная
При низкодозной брахитерапии небольшие штифты, содержащие йод-125 или палладий-103, имплантируются в предстательную железу в качестве источника излучения. Возможна комбинация с чрескожной лучевой терапией. Наиболее частое показание — слабо увеличенная простата (максимально 60 мл) и незначительные симптомы (до 8 баллов по шкале IPSS). После трансуретральной резекции простаты низкодозная брахитерапия связана с более высоким риском развития последующего недержания мочи. Поэтому у пациентов из этой группы рекомендовано рассмотреть другие варианты терапии.
Высокодозная
При высокодозной брахитерапии применяется иридий-192, который вводится в предстательную железу с помощью игл. Чаще всего процедура комбинируется с чрескожной. Протонная терапия, использовавшаяся в недавнем прошлом, не является рутинной процедурой и в настоящее время не дает значимых для пациента преимуществ. Высокодозная брахитерапия в сочетании с чрескожной — основной вариант лечения для пациентов с локально ограниченным раком предстательной железы среднего и высокого профиля риска.
Лучевая терапия при локализованном раке простаты
Низкий риск
Чрескожная лучевая терапия — вариант для первичного лечения клинически локализованного рака простаты. Пациентов с такой опухолью следует облучать чрескожно с дозой не менее 70–72 Гр. Брахитерапия как единственная терапия рекомендуется для первичного лечения клинически локализованного рака простаты с низким профилем риском.
Средний риск
У таких пациентов рекомендуется сочетать чрескожную радиотерапию и гормональную терапию, но надежные научные данные отсутствуют. Пациенты должны получать более высокую дозу облучения (74–80 Гр). Также можно использовать неоадъювантную или адъювантную гормональную терапию, которую рекомендовано назначать краткосрочно — за 3 месяца до начала облучения плюс 3 месяца после процедуры.
Высокий риск
У пациентов с опухолью высокого риска неоадъювантную (за 6 месяцев до начала лучевой терапии) или адъювантную гормональную терапию следует проводить в течение не менее 2 лет в дополнение к облучению, что продлевает выживаемость. Пациенты с опухолью высокого риска не должны получать только брахитерапию: комбинация с чрескожной или гормональной должна проводиться только в рамках исследований.
Лучевая терапия при местно распространенном раке предстательной железы
В сочетании с гормональной терапией чрескожная — вариант первичного лечения местно распространенного рака предстательной железы. Комбинация превосходит монотерапию. Пациентов следует подробно информировать о преимуществах и недостатках этой комбинированной терапии, а также радикальной простатэктомии с лимфаденэктомией. Пациентов с местно распространенным раком предстательной железы необходимо чрескожно облучать не менее 74–80 Гр. В дополнение к чрескожной радиотерапии рекомендуется назначить гормональную терапию — адъювантную или неоадъювантную. Неоадъювантная гормональная терапия должна проводиться в течение 2–3 месяцев, адъювантная — не менее 2 лет; общая продолжительность должна быть не менее 2, лучше 3 года. Эффективность облучения лимфатических путей в малом тазе в дополнение к локальному облучению простаты при локально ограниченном раке предстательной железы со средним и высоким профилем риска еще не может быть окончательно оценена.

Осложнения радиотерапии
При правильном использовании ионизированные лучи и гамма-лучи обеспечивают эффективный и щадящий способ лечения рака. Излучение разрушает ядро раковой клетки, поэтому оно теряет способность делиться. В отличие от здоровых клеток раковые неспособны регенерировать сами, поэтому рост опухоли прекращается. Большое преимущество радиотерапии — местное применение. Ионизирующее излучение действует только там, где есть опухоли или метастазы. Затрагиваются только небольшие участки тела, что снижает риск развития серьезных побочных эффектов. Повреждение тканей при облучении может привести к осложнениям, частота которых, как и при радикальной простатэктомии (РПЭ), уменьшается с опытом лечащего врача и улучшенными методиками. В настоящее время не существует профилактического лечения с помощью медикаментозных средств.
Острые осложнения (в течение трех месяцев). Они встречаются редко. Исключение — брахитерапия, из-за которой у многих пациентов возникают временные проблемы с мочеиспусканием из-за вмешательства на предстательной железе. Тошнота — другой распространенный побочный эффект, с которым можно бороться с помощью сухого хлеба или хлебцев. Проснувшись, можно съесть кусочек поджаренного хлеба. Рекомендуется избегать неприятных запахов пищи и регулярно проветривать помещение, есть медленно и тщательно пережевывать пищу. Если в результате лечения возникает воспаление слизистой оболочки полости рта, можно отказаться от кислой, острой или горькой пищи и газированных напитков. При возникновении запора или диареи рекомендовано употреблять достаточное количество клетчатки и небольшое количество свежих фруктов. Эксперты советуют не употреблять витаминные препараты и пищевые добавки, поскольку большинство полезных веществ можно получить из сбалансированного рациона.
Поздние осложнения. Они встречаются чаще и из-за замедленного действия радиации все еще возможны через несколько лет:
- воспаление мочевого пузыря (цистит);
- примесь крови в моче (гематурия);
- недержание (как правило, позывы из-за раздражения мочевого пузыря);
- рубцевание;
- проктит (воспаление прямой кишки);
- диарея;
- появление крови в стуле;
- отек ног;
- синдром хронической тазовой боли.
Даже если нет видимых изменений после процедур, облученная область тела может оставаться более чувствительной в долгосрочной перспективе. Рекомендуется учитывать возможные перемены при личной гигиене и работе с возможными раздражителями — солнцем, химическими веществами или механическими нагрузками. Особая форма питания не нужна. Рекомендуется избегать жирных и сладких продуктов, поскольку они часто вызывают дискомфорт, а также трудноусвояемых продуктов — фруктов с твердыми скорлупами, газообразующих овощей и мюсли.
Возможные последствия
Серьезные последствия лучевой терапии при раке простаты:
- эректильная дисфункция: поражает примерно одинаковое количество пациентов через год после чрескожной лучевой терапии, брахитерапии и радикальной простатэктомии. В дополнение к повреждению нервов причиной также может быть психика (например, депрессивное настроение);
- вторичные опухоли: радиационное воздействие на окружающие здоровые ткани также увеличивает риск развития вторичной злокачественной опухоли, особенно при раке прямой кишки и мочевого пузыря.
Как диагностируется рецидив
В отличие от радикальной простатэктомии, значение ПСА очень медленно падает до низкого уровня после успешной радиотерапии. После чрескожной лучевой терапии концентрация нормализуется в среднем через 18–36 месяцев, низкодозной брахитерапии – в течение значительно более длительного периода. Часто наблюдается «скачок ПСА». Повышенная концентрация ПСА усложняет диагностику биохимических рецидивов. Если значение поднимается более чем на 2 нг/мл выше надира, что должно быть подтверждено по крайней мере одним дополнительным измерением, это указывает на рецидив. Если у пациента с биохимическим рецидивом после лучевой терапии рассматривается местное лечение, следует попытаться выявить его с помощью трансректальной биопсии простаты. Рекомендуется проводить различие между местным и системным, основываясь на времени удвоения ПСА, времени между лучевой терапией и повышением ПСА и показателем Глисона.
Радиотерапия при рецидиве
Если прогрессирование простатического специфического антигена, скорее всего, не связано с метастазами, спасательная простатэктомия (СПЭ) является вариантом лечения. Опухоль низкого риска, повышение уровня ПСА через 3 с лишним года и высокий уровень более 12 месяцев — показания для простатэктомии. Результаты СПЭ в отношении эректильной дисфункции и недержания мочи, однако, сравнительно хуже, чем при радикальной без предшествующей лучевой терапии. Спасательную простатэктомию следует проводить как можно раньше, и в связи с радиационными изменениями в ткани выполняться она должна только урологом, имеющим многолетний опыт.












