
Все опухоли надпочечников объединяются в группу осложненных эндокринологических патологий, способных проявится в мозге и корковом слое. Среди всех заболеваний, которые относятся к данной группе, кортикостерома диагностируется чаще всего. У 30% больных она способна перерасти в злокачественную опухоль.
Что такое кортикостерома надпочечника
Кортикостерома представляет собой гормонопродуцирующую опухоль надпочечника. Она образуется из коркового вещества и вырабатывает кортизол. Последнее обусловливает симптоматику синдрома Иценко-Кушинга, которой сопровождается патология.
Существуют доброкачественные (аденомы) и злокачественные (аденокарциномы, кортикобластомы) кортикостеромы.
По статистике из всех опухолей на долю злокачественных приходится 57%, остальные – доброкачественные. Большинство опухолей образуется у женщин, в 5 раз больше чем у мужчин.
Код по МКБ 10
Код международной классификации болезней 10 (МКБ-10) злокачественные новообразования надпочечников относятся к категории C74, и дополнительно разделяются по локализации:
- C74.0. Коры надпочечника
- C74.1. Мозгового слоя надпочечника
- C74.9. Надпочечника неуточненной части
Доброкачественные образования этой области относят к категории D35.0 и E24 – синдром Синдром Иценко-Кушинга.
Характеристика кортикостеромы

Вероятность того, что характер опухоли доброкачественный прямо пропорциональна возрасту и обратно пропорциональна ее размеру. Размеры аденом составляет от 1 до 15 см, а вес – от 2 до 200 г. У доброкачественной опухоли присутствует плотная капсула из соединительной ткани, в которой расположено множество кровеносных сосудов.
Злокачественные опухоли нередко обладают внушительными размерами с весом до 1 кг и выше. Они характеризуются плотной бугристой поверхностью, обилием кровеносных сосудов. Цвет варьируется от желтого до темно-вишневого. Образования быстро прорастают в соседние ткани. Формируют метастазы при миграции клеток по лимфатической и кровеносной системе.
Преимущественно первичное образование поражает один надпочечник. Из-за избыточной секреции гормонов второй атрофируется. Это осложняет послеоперационное лечение и требует назначения гормональной терапии.
Наиболее частая локализация вторичных очагов – забрюшинные и парааортальные лимфатические узлы. Они также обладают гормональной активностью, поэтому после операции симптомы проходят не всегда. Последнее указывает на прогрессирование болезни.
Причины и патогенез кортикостеромы
Факторы риска появления новообразования до конца не известны. Среди причин предполагают наследственность воздействие окружающей среды или лекарственных препаратов.
Гормональная активность зависит от вырабатываемого гормона. При синтезе клетками опухоли минералокортикоидов или андрогенов она выражена значительно меньше, чем при выработке глюкокортикоидов. При избыточном количестве последний, снижается выработка АКТГ гипофизом, из-за чего происходят атрофические изменения интактных тканей надпочечников.
Заболевание на клеточном уровне оказывает негативное воздействие на мышечную, костную и соединительную ткань. Дает начало дегенеративным процессам. Наблюдается дисбаланс обмена углеводов, жиров и электролитов. Это приводит к развитию таких заболеваний, как ожирение, стероидный диабет, сердечная недостаточность, нарушения частоты сердечных сокращений, повышение кровяного давления.
Из-за высокого уровня стероидных гормонов в организме происходит сбой деятельности иммунной системы, из-за чего часто возникают инфекции, а процесс выздоровления значительно затягивается.
Симптомы кортикостеромы


К клиническим проявления болезни относят:
- повышенное кровяное давление (сопровождается сердечной недостаточностью и отеками) ;
- мышечная слабость;
- быстрая утомляемость;
- нарушение углеводного обмена (стероидный диабет);
- ожирение (один из первичных симптомов, именно на значительный набор веса в которой срок жалуется большинство пациентов);
- растяжки в области бедер и живота (см. фото выше);
- половые нарушения;
- точечные кровоизлияния;
- остеопороз (ломкость костей).
Болезнь сопровождается нарушением баланса жидкости и электролитов, что проявляется неутолимой жаждой и частыми мочеиспусканиями с повышением общего объема мочи.
Жировые отложения скапливаются в области лица, шеи, живота поясницы, при этом конечности остаются худыми.
У мужчин наблюдается развитие женских вторичных половых признаков – гинекомастия (увеличение молочных желез). Подобное нередко сопровождается уменьшением в размерах полового члена, гипертрофией яичек, снижением половой функции. У женщин болезнь нередко сопровождается огрубением голоса, появление волосяного покрова в необычных местах, увеличением клитера, менструальные нарушения (аменорея и дисменорея).
Могут быть и психоэмоциональные нарушения. У больных наблюдаются эмоциональные расстройства, депрессии, часто болезнь сопровождается потерями памяти.
На коже могут быть обнаружены угри или фолликулы в большом количестве, чрезмерная сухость, точечные кровоизлияния, высыпания, гибок ногтей. В области ног могут формироваться трофические язвы или участки гиперпигментации. Изменяется удельный вес мочи из-за постоянного питья. У трети пациентов развивается хронический пиелонефрит или мочекаменная болезнь. При злокачественной природе опухоли наблюдаются симптомы общей интоксикации.
Диагностика кортикостеромы
Диагностика основывается на внешнем виде больного. Наблюдаются атрофические поражения кожи, костей и мышц. Признаком заболевания считается сахарный диабет и артериальная гипертензия.
Для подтверждения проводится анализ крови на определение уровня АКТГ исследование с дексаметазоном (определение кортизола в сыворотке через 7-8 часов после приема дексаметазона), а также исследование мочи на 17-ОКС и кортизол. Опухоль определяется визуальными методами диагностики (рентгенографией, УЗИ). Проводится магнито-резонансное сканирование головного мозга с введением контрастного вещества. Если опухоль имеет вненадпочечниковую локализацию (вторичный очаг), то постановка диагноза осложняется.
В таком случае симптоматика схожа на кортикостерому, проявляется теми же особенностями при лабораторной диагностике. Но компьютерная томография показывает иной расположение опухолей. Чаще всего они локализуются в грудной клетке (легких).
Лечение и прогноз кортикостеромы
Если обнаружена кортикостерома, лечение – хирургическое. Область вмешательства затрагивает весь надпочечник – его удаляют. Существуют две основные методики проведения – через эндоскопический доступ или лапаротомически (открытым способом).
После удаления органа может развиться надпочечниковая недостаточность, поэтому до конца жизни проводится заместительная терапия гормонами. Дополнительно назначается лечение ингибитором кортикостероидов, он подавляет синтез гормонов метастазами.
Наличие вторичных очагов (выявленных на компьютерной томографии) – показание к проведению химиотерапии. Злокачественные опухоли надпочечников имеют неблагоприятный прогноз (отмечаются только отдельные случаи продолжительной ремиссии), доброкачественные чаще всего излечиваются полностью. Симптомы после удаления ослабевают и через некоторое время полностью пропадают. В течение 15-2 месяцев наблюдаются значительные улучшения:
- нормализуется метаболизм;
- улучшается внешний вид;
- снижается кровяное давление;
- лицо бледнеет;
- половая функция восстанавливается;
- исчезает сахарный диабет, возникший на фоне избыточного продуцирования гормонов.
Уже в первое время после операции (несколько месяцев) наблюдается значительное снижение массы тела, превышающее в некоторых случаях, 20 кг. Проходят боли в костях, но на регенерацию последних уходит до года. В отдаленные сроки у 5-7% больных развивается хроническая недостаточность надпочечников. Основная причина – инфицирование.
Соблюдения специальной диеты при заболеваний и после него не требуется. Питание должно быть разнообразным, пища – богата микроэлементами и минералами (Стол № 15). Наблюдение у эндокринолога после операции и постановка на учет показаны в любом случае.
Вне зависимости от природы происхождения новообразования в надпочечниках, оно может быть опасно вероятными осложнениями нарушения гормонального баланса в организме. Симптомы, способные указывать на подобную патологию требуют обращения к врачу в максимально короткие сроки для проведения всесторонней диагностики и назначения адекватного лечения болезни.
Кортикостерома
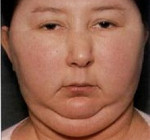
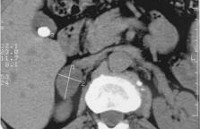
Кортикостерома – опухоль коркового вещества надпочечников, автономно секретирующая избыточное количество кортизола и приводящая к развитию синдрома Иценко-Кушинга. Клинические проявления кортикостеромы характеризуются симптомокомплексом гиперкортицизма: артериальной гипертензией, кушингоидным ожирением, мышечной слабостью, нарушением углеводного обмена и половой функции, явлениями вирилизма (у женщин) и признаками демаскулинизации (у мужчин). Диагностика кортикостеромы включает полипозиционное УЗИ, сцинтиграфию, КТ и МРТ надпочечников, проведение дексаметазоновой пробы, определение уровня кортизола крови и мочи. При обнаружении кортикостеромы требуется хирургическое лечение — адреналэктомия.
- Характеристика кортикостеромы
- Причины и патогенез кортикостеромы
- Симптомы кортикостеромы
- Диагностика
- Лечение кортикостеромы
- Прогноз
- Цены на лечение
Общие сведения
Кортикостерома – опухоль пучковой зоны коркового вещества, в избыточных количествах продуцирующая кортизол, что сопровождается клиникой эндогенного гиперкортицизма – синдрома Иценко-Кушинга. Среди кортикостером в эндокринологии встречаются доброкачественные (аденомы) и злокачественные (аденокарциномы, кортикобластомы) новообразования. Чем старше возраст больного и меньше размер кортикостеромы, тем больше вероятность ее доброкачественного характера. По статистике, злокачественные кортикостеромы встречаются в 57% случаев, доброкачественные — в 43%; у женщин данный вид опухоли обнаруживается в 5 раз чаще, чем у мужчин.

Характеристика кортикостеромы
Большинство кортикостером развиваются в пучковой зоне коры одного из надпочечников. Возможно произрастание кортикостеромы из эктопированной надпочечниковой ткани в почках и яичниках. Размеры доброкачественных аденом составляют 1-15 см, вес — 2-200 гр. Доброкачественные кортикостеромы покрыты плотной капсулой из соединительной ткани с обильной васкуляризацией.
Аденокарциномы и кортикобластомы могут достигать гигантских размеров и веса 800 — 1200 гр. Злокачественные кортикостеромы имеют бугристую плотную поверхность с большим количеством сосудов; на разрезе опухоли выявляются участки некрозов и кровоизлияний, из-за чего опухолевая ткань приобретает пеструю окраску с чередованием зон желтого и темно-вишневого цвета. Инфильтративный рост злокачественных кортикстером приводит к прорастанию околопочечной клетчатки, магистральных сосудов и поражению соседних органов. Метастазирование опухоли происходит по лимфатическим и кровеносным путям в забрюшинные и парааортальные лимфоузлы, легкие и печень. Метастазы кортикостеромы также обладают гормональной активностью и могут продолжать синтезировать кортизол даже после удаления основной опухоли.
Причины и патогенез кортикостеромы
Этиология и факторы риска опухолей надпочечников изучены недостаточно. Среди вероятных причин развития кортикостеромы рассматриваются наследственность, агрессивные факторы среды, воздействие отдельных видов лекарственных средств. Гормональная активность кортикостеромы проявляется в избыточном синтезе глюкокортикоидов, в меньшей степени – минералокортикоидов и андрогенов. При избытке глюкокортикоидов по механизму обратной связи снижается синтез АКТГ гипофизом, вследствие чего интактные ткани надпочечников подвергаются атрофическим изменениям.
Биологические эффекты эндогенного гиперкортицизма на тканевом уровне характеризуются катаболическим действием на костную, мышечную и соединительную ткань, что сопровождается системными дистрофическими процессами. Грубо нарушается протекание углеводного (гипергликемия), жирового и электролитного обмена (гипернатриемия и гипокалиемия), вследствие чего возникают стероидный диабет, ожирение, артериальная гипертензия, сердечная недостаточность, аритмии. Иммуносупрессивное действие глюкокортикоидов проявляется склонностью к инфекциям.
Симптомы кортикостеромы
Клиническая картина кортикостеромы обусловлена эндогенным гиперкортицизмом, приводящим к изменениям со стороны различных органов. К ранним и стабильным признакам кортикостеромы относятся кушингоидное ожирение, артериальная гипертензия, миастения, головная боль, нарушение толерантности к глюкозе. Нарушения водно-электролитного обмена проявляются полидипсией, полиурией, снижением удельного веса мочи.
На коже молочных желез, живота, внутренних поверхностей бедер появляются петехиальные кровоизлияния, багрово-синюшные стрии. Нередки гнойничковые высыпания — угри, фолликулиты; на нижних конечностях образуются очаги гиперпигментации и трофические язвы. У женщин кортикостерома вызывает явления вирилизации: гирсутизм, снижение тембра голоса, дисменорею и аменорею, гипертрофию клитора. У мужчин с кортикостеромой обнаруживаются признаки демаскулинизации – гинекомастия, гипоплазия яичек, снижение потенции.
У значительной части пациентов развивается остеопороз, нередко приводящий к патологическим переломам ребер, компрессионным переломам позвоночника. В трети случаев течению кортикостеромы сопутствуют хронический пиелонефрит и мочекаменная болезнь. Возможно развитие психически нарушений — возбуждения, депрессии. Злокачественная кортикостерома, кроме синдрома Кушинга, сопровождается интоксикацией, характерной для онкологических опухолей.
Диагностика
Ведущая роль в диагностике кортикостеромы принадлежит определению кортикостероидных гормонов и их метаболитов в сыворотке крови и моче. Для дифференциации кортикостеромы с АКТГ-эктопическим синдромом и болезнью Иценко-Кушинга проводится большая дексаметазоновая проба (проба Лиддла) с последующим определением кортизола и АКТГ. При кортикостероме после приема дексаметазона уровень кортизола крови и экскреция 17-ОКС не снижаются; повышение АКТГ в плазме крови рассматривается как проявление АКТГ-эктопического синдрома.
С целью топической диагностики кортикостеромы проводится комплекс визуализирующих исследований:
Для оценки изменений со стороны других органов и систем организуются консультации кардиолога, уролога-андролога, гинеколога, невролога.
Лечение кортикостеромы
Выявление кортикостеромы служит абсолютным показанием к хирургическому удалению опухоли. При кортикостероме производится удаление надпочечника (адреналэктомия) открытым или эндовидеохирургическим методом. Для профилактики надпочечниковой недостаточности в раннем послеоперационном периоде проводится заместительная гормонотерапия.
После удаления злокачественной кортикостеромы с целью подавления гормональной активности возможных отсевов опухоли дополнительно назначаются ингибиторы секреции кортикостероидов (митотан). При клинически и рентгенологически подтвержденных метастазах требуется проведение химиотерапии.
Прогноз
Удаление доброкачественных кортикостером способствует постепенному регрессу клинической симптоматики: изменению внешнего облика, нормализации АД и обменных процессов, побледнению стрий, восстановлению половой функции, исчезновению стероидного диабета, снижению массы тела, восстановлению костной ткани и т. д. В послеоперационном периоде пациентам показано диспансерное наблюдение эндокринолога. При злокачественной кортикостероме прогноз неблагополучный.
Кортикостерома
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК — 2017
Общая информация
Краткое описание
Кортикостерома – гормонально активная опухоль из клеток коры надпочечников (преимущественно пучковой зоны), продуцирующая в избыточном количестве глюкокортикоиды, что приводит к развитию эндогенного гиперкортицизма [1].
NB! Кортикостерома – один из вариантов клинического синдрома Кушинга.
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| Е24 | Синдром Иценко-Кушинга |
Дата разработки/пересмотра протокола: 2017 год.
Сокращения, используемые в протоколе:
| АГ | – | артериальная гипертония |
| АКТГ | – | адренокортикотропный гормон |
| БИК | – | болезнь Иценко-Кушинга |
| ЭГ | – | эндогенный гиперкортицизм |
| МПД | – | малая проба с дексаметазоном |
| УЗИ | – | ультразвуковое исследование |
| МСКТ | – | мультиспиральная компьютерная томография |
| МРТ | – | магнитно-резонансная томография |
Пользователи протокола: эндокринологи, хирурги.
Категория пациентов: взрослые.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |

— Профессиональные медицинские справочники. Стандарты лечения
— Коммуникация с пациентами: вопросы, отзывы, запись на прием
Скачать приложение для ANDROID / для iOS

— Профессиональные медицинские справочники
— Коммуникация с пациентами: вопросы, отзывы, запись на прием
Скачать приложение для ANDROID / для iOS
Классификация
Классификация синдрома Кушинга [2]:
Синдром Кушинга встречается в двух вариантах:
· АКТГ-зависимый;
· АКТГ-независимый.
АКТГ-зависимые формы: болезнь Иценко-Кушинга и синдром эктопической секреции АКТГ.
АКТГ-независимые формы первичную опухоль надпочечников (аденома, рак) или узелковую их гиперплазию.
Классификация кортикостером (по морфо-функциональным признакам):
· светлоклеточные;
· темноклеточные;
· смешанноклеточные;
· гигантоклеточные.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Жалобы и анамнез:
· появление в течение короткого времени центрального ожирения;
· багрово-синюшных стрий;
· АГ;
· у женщин – симптомов вирилизации;
· у мужчин – снижения либидо и потенции.
Физикальное обследование:
· наиболее ранними и постоянными проявлениями заболевания считают центральное (кушингоидного) ожирение, АГ (90-100 %), головную боль, мышечную слабость и быструю утомляемость;
· у 40-90% имеет место нарушение углеводного обмена (нарушение толерантности к глюкозе или стероидный диабет);
· у 70% женщин – симптомы вирилизации (гипертрихоз, огрубение голоса, дисменорея, аменорея);
· у 85% мужчин – снижение либидо и потенции;
· частый признак – синюшно-багровые стрии на коже живота, молочных желез и внутренних поверхностей бедер, петехиальные кровоизлияния;
· у 80% – компрессионные переломы тел позвонков вследствие остеопороза. У 15% пациентов выявляют мочекаменную болезнь, хронический пиелонефрит. Нередко развиваются психические нарушения (возбуждение, депрессия). Может иметь место почечная колика.
Лабораторные исследования [3]:
перед проведением любых лабораторных исследований необходимо исключить введение экзогенных глюкокортикоидов.
Проведение лабораторных исследований направлено, во-первых, на выявление факта гиперкортизолемии (эндогенного гиперкортицизма), во-вторых, на уточнение ее генеза — дифференциальную диагностику АКТГ – зависимого и АКТГ – независимого ЭГ (таблица 1).
Таблица – 1. Диагностические тесты, которые применяются для первичной диагностики ЭГ*.
| Тесты первой линии | Чувствительность (%) | Специфичность (%) |
| определение АКТГ и кортизола в плазме крови | 95 | 80 |
| определение свободного кортизола в слюне | 90 | 90 |
| малая проба с дексаметазоном (МДП) (1мг) | 95 | 80 |
| определение свободного кортизола в суточной моче | 80 | 80 |
| определение кортизола в сыворотке крови вечером | 90 | 90 |
*Проведение большой пробы Лиддла в настоящее время не рекомендуется.
При выборе диагностических тестов первой линии важно учитывать возможность их проведения в амбулаторных условиях, их диагностическую информативность.
Для первоначального скрининга на ЭГ рекомендуются:
· определение АКТГ и кортизола в плазме крови (для дифференциальной диагностики АКТГ-зависимого и АКТГ-независимого ЭГ);
· определение уровня свободного кортизола в образце слюны, собранной пациентом в 23:00 (отражает нарушение циркадности продукции кортизола);
· малая проба с дексаметазоном (МПД): исследование кортизола в сыворотке крови утром после приема в 23:00 накануне 1 мг дексаметазона (подавление секреции АКТГ и кортизола в ответ на введение дексаметазона исключает наличие кортиостеромы);
· определение уровня свободного кортизола в суточной моче (отражает суточную секрецию кортизола);
Наиболее удобным неинвазивным методом диагностики эндогенного гиперкортицизма является определение кортизола в слюне, собранной в 23:00. Сбор слюны выполняется самостоятельно пациентом в амбулаторных условиях. Слюна содержит свободный, стабильный при комнатной температуре до 7 дней кортизол, уровень которого не зависит от содержания кортизол-связывающего глобулина (можно использовать у женщин, получающих гормональные контрацептивы и гормональную заместительную терапию) и количества слюны, что дает преимущество перед определением свободного кортизола в суточной моче, когда потеря части мочи влияет на результат.
Небольшое выделение крови, вследствие интенсивной чистки зубов не влияет на уровень кортизола в слюне.
Таблица – 2. Практические вопросы проведения наиболее информативных и рекомендуемых тестов для первичной лабораторной верификация ЭГ.
| Диагностический тест | Правила проведения и сбора биологического материала | Ограничения существующего метода |
| Определение свободного кортизола в суточной моче | Сбор мочи начинается с пустого мочевого пузыря (первую утреннюю порцию мочи выливают), затем собираются все порции мочи, в том числе первая утренняя порция на следующий день. Собираемая моча должна находиться в холодильнике, не в морозильном отделении. Общий объём мочи измеряется с точностью до 50 мл. | · потери мочи более 50 мл влияют на результат; · употребление более 5 литров жидкости в сутки достоверно увеличивает содержание свободного кортизола в моче; · ухудшение функции почек уменьшает содержание кортизола в моче. Ложно – отрицательный результат наблюдается при снижении клиренса креатинина ниже 60мл/мин, далее содержание кортизола в моче линейно снижается по мере ухудшения функции почек. · кортизол в суточной моче выше у пациентов, принимающих карбамазепин, фенофибрат и синтетические глюкокортикоиды. |
| Малая проба с дексаметазоном | Дексаметазон в дозе 1 мг пациент принимает между 23.00-24.00. Образец крови на определение кортизола берется на следующее утро между 8.00-9.00. Использование более высоких доз дексаметазона не улучшает диагностические возможности теста | · любые нарушения во всасывании и метаболизме дексаметазона; · препараты, усиливающие метаболизм дексаметазона (фенобарбитал, фенитонин, карбамазепин, рифапентин, рифампицин, этосуксимид, пиоглитазон и др.); · препараты, замедляющие метаболизм дексаметазона (апрепитант, итраконазол, ритонавир, флуоксетин, дилтиазем, циметидин и др.); · серьёзная патология печени и почек. |
| Исследование свободного кортизола в слюне, собранной вечером (23:00) | Сбор слюны производится в 23.00 перед сном в спокойной обстановке. В течение 30 минут до сбора слюны нельзя употреблять пищу, пить что-либо кроме простой воды или чистить зубы. Пробирка со слюной помещается в холодильник (не в морозильное отделение), образец стабилен в течение 7 дней. | Искажают результат: · жевательный табак или курение перед забором слюны; · работа в ночное время; · частая смена часовых поясов; · сильная кровоточивость десен. |
Дополнительные методы исследования (биохимический анализ крови, общий анализ крови, общий анализ мочи и др. – по показаниям) позволяют выявить:
· гиперальдостеронемию;
· гипокалиемию;
· гипернатриемию;
· гипергликемию;
· гиперазотемию;
· гиперхолестеринемию;
· гипертриглицеридемию;
· алкалоз.
ОАК:
· нейтрофильный лейкоцитоз со сдвигом влево ??
· лимфоцитопению и эозинопению
· эритроцитоз
ОАМ:
· щелочная реакция мочи
· лейкоцитурия
· глюкозурия
Инструментальные исследования [3]:
· УЗИ надпочечников – характерно выявление округлого образования в одном из надпочечников – информативная ценность 60-80%;
· МСКТ надпочечников – выявляют некрозы и кровоизлияния в больших или гетерогенных опухолях с зонами низкой плотности, кальцификацию опухоли (указывает на рак и/или наличие отдаленных метастазов) – чувствительность 98%;
· МРТ надпочечников – чувствительность метода 86-98%;
· сцинтиграфия с I131 — нор-холестерином (обнаружение одного надпочечника из-за атрофии второго подтверждает диагноз кортикостеромы).
Показания для консультации специалистов:
· консультация хирурга – для определения показаний к оперативному лечению;
· консультация онколога – при подозрении на рак надпочечника.
Диагностический алгоритм:
Схема-1

Кортикостерома надпочечника: симптомы и лечение
Кортикостерома – это доброкачественное или злокачественное новообразование, формирующееся при патологическом разрастании клеток пучковой зоны коры надпочечников. Данная опухоль относится к числу гормонально активных. В ней протекает автономный синтез кортизола. Переизбыток этого биологически активного соединения становится причиной развития гиперкортицизма, известного как синдром Иценко-Кушинга.
Согласно данным медицинской статистики, кортикостеромы в 5 раз чаще диагностируются у женщин.
Характеристики опухоли
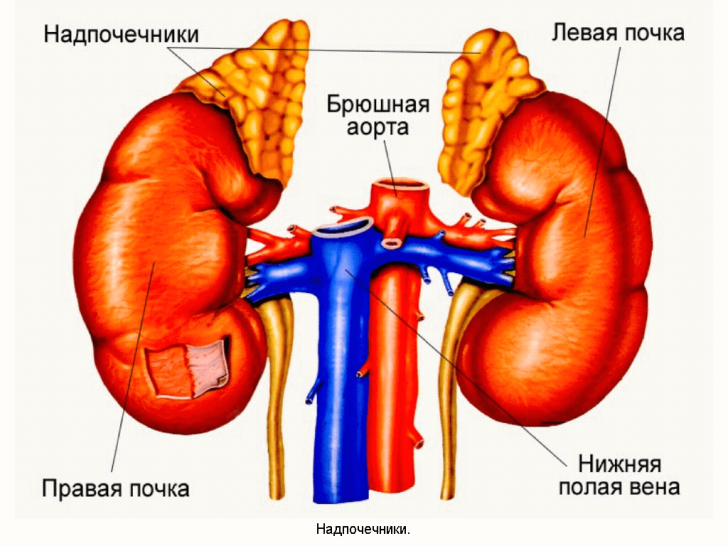
Важно: чем старше пациент, и чем меньше объем опухоли, тем выше вероятность, что характер кортикостеромы доброкачественный, т. е. речь идет об аденоме. На долю таких новообразований приходится порядка 43%. К злокачественным кортикостеромам относятся кортикобластомы и аденокарциномы надпочечников.
Размеры аденом варьируют от 1 до 15 см, а масса – от 2 до 200 граммов. Отличительная особенность доброкачественных опухолей коры надпочечников – наличие плотной соединительнотканной капсулы, пронизанной множеством кровеносных сосудов.
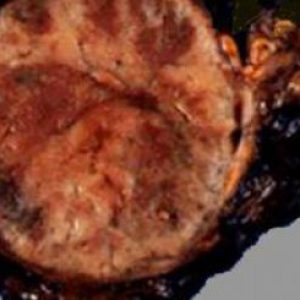 Злокачественные кортикостеромы зачастую достигают огромных размеров, а их вес может составлять свыше 1 кг. У аденокарцином и кортикобластом плотная бугристая поверхность. Для таких новообразований характерен инфильтративный рост с прорастанием в окружающую почки клетчатку, расположенные рядом органы и крупные кровеносные сосуды. Вторичные опухолевые очаги образуются при миграции клеток опухоли гематогенным и лимфогенным путем. Метастазы формируются преимущественно в парааортальных и забрюшинных лимфатических узлах.
Злокачественные кортикостеромы зачастую достигают огромных размеров, а их вес может составлять свыше 1 кг. У аденокарцином и кортикобластом плотная бугристая поверхность. Для таких новообразований характерен инфильтративный рост с прорастанием в окружающую почки клетчатку, расположенные рядом органы и крупные кровеносные сосуды. Вторичные опухолевые очаги образуются при миграции клеток опухоли гематогенным и лимфогенным путем. Метастазы формируются преимущественно в парааортальных и забрюшинных лимфатических узлах.
Обратите внимание: для метастазов также свойственна гормональная активность; они способны продуцировать избыточное количество кортизола даже после успешной операции по резекции основной кортикостеромы.
Причины и патогенез
Истинные причины развития кортикостером к настоящему моменту времени неясны.
К предрасполагающим факторам эндокринологи и онкологи относят:
- генетически обусловленную предрасположенность;
- прием некоторых фармакологических препаратов;
- агрессивные факторы внешней среды (загрязненная атмосфера, ионизирующее излучение и т. д.).
В кортикостеромах преимущественно синтезируются глюкокортикоидные гормоны, но опухоли способны также продуцировать андрогены (мужские половые гормоны) и минералокортикоиды. Высокий уровень глюкокортикоидов в крови пациента запускает механизм обратной связи, что ведет к снижению продукции гипофизом адренокортикотропного гормона. Следствием данного патологического процесса становятся атрофические изменения в неповрежденных структурах надпочечников.
Избыток кортизола активизирует системные катаболические процессы, на фоне которых мышечная, костная и соединительная ткань подвергаются дистрофическим изменениям.
При данной патологии серьезно страдает водно-солевой (электролитный) обмен, а также метаболизм липидов и углеводов. В крови падает уровень калия и повышается содержание натрия.
Последствия метаболических нарушений:
Гормоны-глюкокортикоиды подавляют общий иммунитет, вследствие чего пациенты с кортикостеромами в большей степени подвержены заболеваниям инфекционного генеза.
Симптомы кортикостеромы надпочечника
Клинические проявления гиперкортицизма:
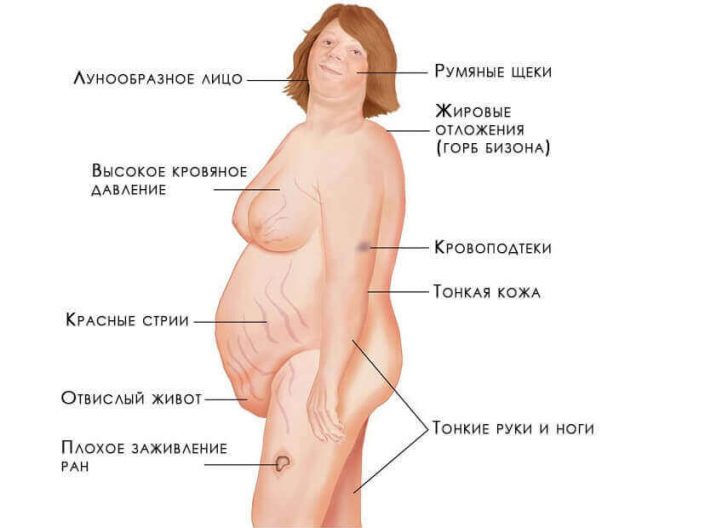 артериальная гипертензия (повышенное АД);
артериальная гипертензия (повышенное АД);- слабость мускулатуры;
- повышенная физическая и умственная утомляемость;
- характерное (центрипитальное) ожирение;
- нарушение метаболизма углеводов (не исключен стероидный диабет);
- нарушения половой функции;
- багровые стрии (растяжки) на коже живота и бедер;
- точечные кровоизлияния (петихии);
- остеопороз (его возможное следствие – компрессионные переломы позвонков).
Водно-электролитный дисбаланс становится причиной неутолимой жажды и увеличением диуреза (со снижением удельной плотности мочи).
Важно: для пациентов мужского пола характерна демаскулинизация – развитие гинекомастии, снижение либидо и потенции, гипоплазия тестикул. У женщин отмечаются признаки вирилизма – гирсутизм (нетипичное оволосение), огрубение голоса и гипертрофия (увеличение) клитора.
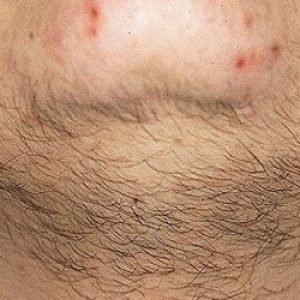 На кожных покровах больных часто появляются гнойничковые высыпания – банальные угри (акне) или фолликулиты. На ногах могут формироваться трофические язвы и зоны гиперпигментации.
На кожных покровах больных часто появляются гнойничковые высыпания – банальные угри (акне) или фолликулиты. На ногах могут формироваться трофические язвы и зоны гиперпигментации.
Почти треть пациентов с гиперкортицизмом страдают от хронического пиелонефрита и мочекаменной болезни.
Важно: для аденокарцином и кортикобластом характерны признаки общей интоксикации.
Диагностика
Важным диагностическим критерием кортикостеромы является сочетание ярких проявлений гиперкортицизма в сочетании с повышением суточного выделения свободного кортизола (определяется в анализах мочи). Оценивается и уровень содержания данного гормона в крови пациента.
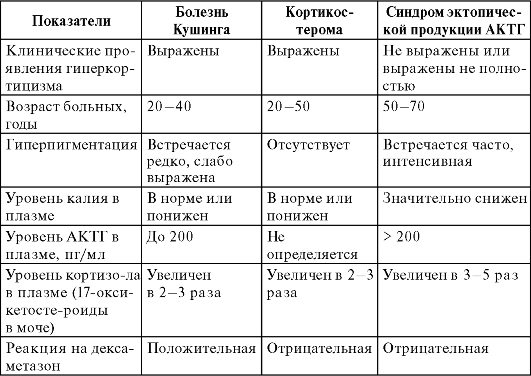
Наиболее информативным лабораторным методом считается дексаметазоновая проба с оценкой уровня АКТГ и кортизола. Она позволяет дифференцировать кортикостерому и болезнь Иценко-Кушинга (нейроэндокринное заболевание, не связанное с новообразованиями).
Для верификации диагноза применятся аппаратные методы исследования – сцинтиграфия (визуализация с предварительным введением контраста – радиоактивного изотопа), полипозиционное ультразвуковое сканирование, магнитно-резонансная и компьютерная томография.
Лечение кортикостеромы надпочечников и прогноз
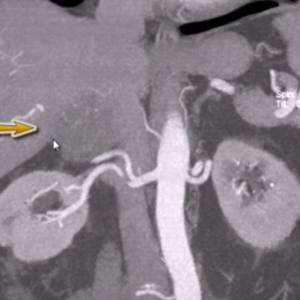 Выявление кортикостеромы является показанием для хирургического вмешательства – адреналэктомии (удаления пораженного опухолью надпочечника).
Выявление кортикостеромы является показанием для хирургического вмешательства – адреналэктомии (удаления пораженного опухолью надпочечника).
Операция проводится открытым доступом или с помощью эндоскопической методики.
Чтобы предупредить развитие надпочечниковой недостаточности, непосредственно после адреналэктомии пациентам показана заместительная гормональная терапия.
Для того чтобы подавить продуцирование гормонов метастазами, после удаления злокачественного новообразования дополнительно проводят лечение Митотаном (ингибитор кортикостероидов). Если рентгенологически подтверждено наличие вторичных опухолевых очагов, пациенту назначается курс химиотерапии цитостатиками.
При диагностированных аденокарциномах и кортикобластомах прогноз, к сожалению, неблагоприятный. Удаление новообразований доброкачественного характера приводит к постепенному снижению выраженности и даже полному купированию симптомов.
Всем пациентам, перенесшим операцию по поводу кортикостеромы, показано диспансерное наблюдение у эндокринолога.
Плисов Владимир, медицинский обозреватель
7,352 просмотров всего, 1 просмотров сегодня
Глюкостерома

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Код по МКБ-10
- Патогенез
- Симптомы
- Диагностика
- Что нужно обследовать?
- Как обследовать?
- Какие анализы необходимы?
- К кому обратиться?
Глюкостерома встречается у 25-30 % больных с признаками тотального гиперкортицизма. Среди других корковых опухолей она также наиболее распространена. Больные этой группы по своему состоянию относятся к наиболее тяжелым. Почти у половины больных опухоль злокачественная. Если у женщин преобладают (в 4-5 раз чаще, чем у мужчин) доброкачественные аденомы, то злокачественные опухоли встречаются с одинаковой частотой у лиц обоего пола. Нарастание симптомов и само развитие болезни не зависят от размера опухоли, имеет значение только ее гормональная активность.
 [1]
[1]
Код по МКБ-10
Патогенез
Глюкостеромы обычно солитарные и односторонние, редко могут быть двусторонними. Размеры опухолей варьируют от 2-3 до 20-30 см в диаметре и более; соответственно колеблется их масса: от нескольких граммов до 2-3 кг. Между размером, массой и характером роста опухоли существует определенная зависимость. Если ее масса до 100 г и диаметр — до 5 см, то она, как правило, доброкачественная; опухоли большего размера и большей массы — злокачественные. Доброкачественные и злокачественные кортикостеромы встречаются примерно с одинаковой частотой. Часть опухолей занимает промежуточное положение по характеру роста.
Аденомы коры надпочечника (глюкостеромы) часто округлой формы, покрыты хорошо васкуляризированной тонкой фиброзной капсулой, сквозь которую просвечивают охряно-желтые участки атрофированной коры надпочечника. Они обычно мягкие, блестящие на разрезе, часто крупнодольчатого строения, пестрого вида: охряно-желтые участки чередуются с красно-коричневыми. Даже в маленьких опухолях могут встречаться некрозы и кальцификаты. Свободные от опухоли участки надпочечника имеют выраженные атрофические изменения в корковом слое.
Микроскопически охряно-желтые участки образованы крупными и мелкими спонгиоцитами, цитоплазма их богата липидами, особенно связанными холестерином. Формируют эти клетки тяжи и альвеолы, реже — участки солидного строения. Зоны красно-коричневого цвета образованы компактными клетками с резко оксифильной цитоплазмой, бедной или не содержащей липиды. Морфологические признаки активной пролиферации опухолевых клеток, как правило, отсутствуют, но рост опухоли, наличие многоядерных клеток и т. д. свидетельствуют о том, что они активно делятся, очевидно амитотически. Встречаются также экземпляры, особенно у больных с повышенным уровнем андрогенов в крови, с примесью клеток, сходных с клетками сетчатой зоны. Они содержат липофусцин и формируют структуры, напоминающие сетчатую зону коры. В отдельных опухолях имеются участки, образованные элементами клубочковой зоны. У таких больных развиваются и явления гиперальдостеронизма. Очень редко аденомы целиком образованы клетками с оксифильной цитоплазмой, содержащей разнообразное количество липофусцина. Присутствие этого пигмента придает опухоли черный цвет. Такие аденомы называются черными.
Злокачественные опухоли обычно крупные, массой от 100 г до 3 кг и более, мягкие, покрытые тонкой, богато васкуляризованной капсулой. Под ней обнаруживаются островки атрофированной коры надпочечника. На разрезе они пестрого вида с многочисленными участками некрозов, кровоизлияний свежих и старых, кальцификатов, кистозными участками с геморрагическим содержимым крупнодольчатого строения. Дольки разделены прослойками фиброзной ткани. Микроскопически раки отличаются значительным полиморфизмом как по структуре, так и по цитологическим особенностям.
В надпочечнике, содержащем опухоль, и в контралатеральном надпочечнике наблюдаются выраженные атрофические изменения. Кора образована в основном светлыми клетками, капсула утолщена, нередко отечна. В местах локализации опухоли кора практически полностью атрофирована, сохраняются лишь единичные элементы клубочковой зоны.
Патологоанатомические изменения во внутренних органах, в костях скелета, в коже, мышцах и т. д. сходны с изменениями, наблюдаемыми при болезни Иценко-Кушинга.
В редких случаях кортизолсекретирующие аденомы коры надпочечника сочетаются с АКТГ-продуцирующими аденомами гипофиза или фокальной гиперплазией АКТГ-продуцирующих клеток гипофиза.












